III- L'homme a-t-il le meme avenir que les especes immortelles?
Nous avons vu précédemment que l’Homme bénéficie de certains facteurs extérieurs qui lui permettent d’augmenter son espérance de vie et de retarder l’heure fatidique. Cependant, certaines espèces ont repoussé les limites de la mort à l’extrême, frôlant (et même atteignant pour certaines) l’immortalité.
Quelles sont ces espèces et quelles sont leurs ressemblances et divergences par rapport à l’homme ?
1- Les êtres vivants qui défient la mort
-La Bactérie Arthrobacter
Dans des conditions défavorables, la bactérie est capable de se mettre en dormance et de libérer des spores. Les spores sont des organites spécifiques très résistants qui peuvent survivre de très longues périodes (environ 1000 ans) dans des conditions environnementales (de température par exemple) extrêmes. Elles contiennent une copie du génome de la cellule mère. Lorsque les conditions s’améliorent, ces spores peuvent donner naissance à de nouvelles bactéries. C’est ce qu’on appelle la germination. Ceci est possible grâce à une enzyme, Spore Photoproduct Lyase (SPL). Cette enzyme répare les lésions qui adviennent dans l’ADN bactérien. D’autres bactéries non sporifères ont un métabolisme réduit capable de réparer seul l’ADN, ce qui fait qu’elles vivent aussi longtemps.
Cependant, ce mécanisme de réparation de l’ADN n’est pas immortel. Il s’abimerait avec le temps. Ceci classe donc la bactérie Arthrobacter parmi les espèces qui défient la mort.

Bactérie Arthrobacter
-L’hydre
Lorsqu’une partie de son organisme est amputée, le corps la régénère en 2 ou 3 jours. L’hydre serait donc potentiellement immortel. En effet, l’hydre renfermerait dans la partie centrale de son corps des cellules souches au potentiel supérieur aux cellules souches d’un mammifère (homme inclus) à l’âge adulte. En cas de lésion, ces cellules souches se différencient afin de former les cellules manquantes et reconstruire la partie amputée.

Phénomène de Différenciation
Il se peut donc que la partie centrale de l’hydre contiennent des cellules souches qui vieillissent peu ou pas et que ses extrémités déclinent mais sont remplacée par les descendantes des cellules souches.

- Les conifères
De tous les êtres vivants, les arbres sont ceux qui vivent le plus longtemps. Selon des chercheurs du laboratoire de physiologie végétale de l’université d’Oviedo en Espagne, certains arbres comme les pins ne vieilliraient pas. En effet, cela s’explique par le phénomène de déméthylation.
→ la méthylation est un mécanisme chimique qui advient chez l’homme. Il consiste au rajout d’un méthyle (groupement carboné) qui se fixe sur un nucléotide. Ce groupement méthyle empêche la régénération de certaines cellules et empêche le gêne de s’exprimer car elles empêchent toute interaction entre gène et protéine.
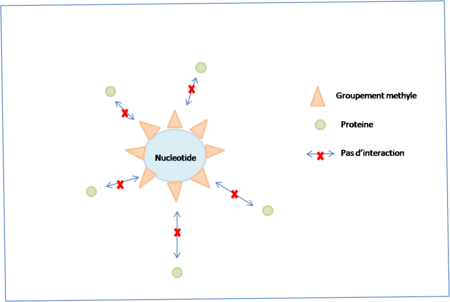
Phénomène de methylation
Chez les cèdres, le phénomène qui se produit est la déméthylation.
Chez l’arbre, durant sa croissance hivernale ralentie, de la déméthylase est secrétée. La déméthylase est une enzyme permettant de retirer le radical méthyle qui empêchait la cellule de se régénérer.
Si la méthylation empêche un gène de s’exprimer, la déméthylation « casse » le groupement méthyle et permet au gène de s’exprimer, et aux cellules de se régénérer.

Phénomène de demethylation
2- Les êtres vivants qui vainquent la mort
- La méduse Turritopsis Nutricula
Recensée pour la première fois en 1883 dans la Mer Méditerranée, la méduse Turritopsis Nutricula mesure quelques 5 mm à peine (à l’âge adulte, elle fait la taille d’un ongle). Son invasion maritime silencieuse a été difficile à repérer car elle change d’aspect physique selon la région où elle se trouve. En effet, celles qui vivent dans les eaux tropicales ont 8 tentacules, alors que celles qui vivent dans les régions tempérées en ont 24.


Turritopsis Nutricula à 8 tentacules Turritopsis nutricula à 24 tentacules
Maria Pia Miglietta, biologiste à l’université de Pennsylvanie, est spécialiste des hydrozoaires, la classe des cnidaires à laquelle appartient la méduse. Elle s’est intéressée à la phylogénie (étude de la formation et de l’évolution d’une espèce) des méduses. Elle a étudié leur génome afin de retracer l’évolution des différentes espèces en vu d’établir leur lien de parenté.
Elle s’est concentrée sur un gène unique utilise d’habitude pour reconnaitre ce genre de meduse : le gène mitochondrial 16S. Elle l’a comparé à différents échantillons recueillis autour du globe et a remarqué que le gène est rigoureusement le même chez toutes les espèces étudiées.
Cette méduse est extrêmement fragile, et, notons-le bien, est capable de mourir. En effet, une simple bulle d’air suffit à la faire éclater. Comment un être vivant si vulnérable peut-il alors traverser les océans entiers ?
En fait, la méduse Turritopsis Nutricula se fixe dans les ballasts des navires. Lorsqu’elle se retrouve en danger ou dans une situation critique, elle est capable d’inverser son cycle de vie.
Quel est le cycle de vie de la méduse ?
La méduse a deux phases de vie :une phase fixe (le polype) et une phase adulte (la méduse elle-même).
La méduse naît sous la forme de polype. Le polype est en fait forme d’une multitude de petits bourgeons, qui, au milieu de l’année, se détachent du polype et donnent naissance à des mini-méduses qui grandissent. À l’âge adulte, la méduse a le choix : elle peut se reproduire (mâles et femelles lâchent leurs spermatozoïdes et leurs œufs dans la mer) puis de mourir. Elle peut aussi choisir d’inverser son cycle de vie et de revenir au stade de bourgeon.
Elle est, à ce jour, le seul organisme pluricellulaire capable de revenir à un stade juvénile après avoir atteint sa maturité sexuelle. Cela est permis par un processus cellulaire très particulier : la transdifferenciation.
La différenciation étant la spécialisation de cellules (en cellules nerveuses, cardiaques…), la transdifferenciation est le passage d’une cellule de son état spécialisé à son état original indifférencié.

Cycle de vie de Turritopsis Nutricula.
3- Quel avenir pour l’homme ?
L’équipe japonaise de Shinya Yamanaka a deposé le 1er brevet du monde pour protéger leur découverte de 2006 sur la reprogrammation des cellules souches.
Ils ont tente de différencier les cellules souches pour qu’elles soient aussi versatiles que les cellules souches embryonnaires.
Comme la plupart des cellules, les cellules souches expriment des gènes particuliers et spécifiques. L’idée de Yamanaka est de chercher parmi ces gènes des gènes maîtres qui contrôlent le destin cellulaire. Si on exprime artificiellement ces gènes maîtres dans une cellule adulte, l’espoir est qu’ils reprogramment la cellule et lui ordonnent de redevenir cellule souche. Yamanaka sélectionne 24 gènes connus pour être exprimés dans les cellules souches chez la souris. Il pense que parmi ces 24 gènes se trouvent les gènes maîtres des cellules souches, ceux qui contrôlent le destin cellulaire. Il prend alors des copies de ces 24 gènes, les intègre dans le génome de cellules de souris adultes avec un rétrovirus pour les surexprimer. Au bout de quelques jours, plusieurs cellules adultes reviennent à l’état de cellules souches. Il doit alors identifier la combinaison minimale des gènes, et finit avec 4 gènes appelés Oct3/4, Sox2, Klf4 et c-Myc. Les cellules adultes retournent à l’état de cellules souches, et Yamanaka montre qu’elles sont également capables de se redifférencier en n’importe quel type de cellule : elles sont donc bien pluripotentes. Il les baptise alors « cellules souches pluripotentes induites » (iPS).
-Qu’est-ce qu’une cellule iPS ?
Une cellule IPS est une cellule souche pluripotente (de l’anglais : induced pluripotent stem cell) qui se comporte comme les cellules souches embryonnaires. Elle en est différente par son origine : en effet, les cellules souches embryonnaires proviennent de l’embryon, alors que les cellules souches IPS proviennent de cellules adultes spécialisées qui se sont dédifférenciées.
-Quelle est la différence avec les cellules souches adultes ?
Les cellules souches adultes (comme celles de la moelle épinière) sont déjà partiellement différenciées. En fait, une cellule souche de la moelle épinière peut se différencier en une cellule sanguine, mais pas en un neurone. Les cellules IPS ne sont pas du tout différenciées. Elles peuvent donner naissance à n’importe quel type de cellule.
Le seul problème est que les cellules souches ont un génome modifié et peuvent potentiellement provoquer des cancers.
Comment ces 4 facteurs insérés peuvent-ils causer le cancer ?
Il existe en fait dans la cellule un gène suppresseur de tumeur : le gène P53. Ce gène arrête les cellules devenues cancérigènes, mais fait aussi barrière à la reprogrammation des cellules adultes en cellules souches. Lors de l’expérience menée par l’équipe de Yamanaka, peu de cellules souches ont pu se dédifférencier en cellules iPS : les deux facteurs oncogènes Kil 4 et c-myc ont active le gène P53 qui a bloqué la reprogrammation de la cellule. Si on inactive le gène P53, la reprogrammation serait dix fois plus rapide et ne nécessitera pas de stimulants oncogènes. Cependant, il y aura un grand risque de cancer car la gène P53 est le gardien de la stabilité du chromosome.
D’après les papiers de fin 2007, on peut appliquer la même technique aux cellules humaines. La prochaine étape est d’arriver à fabriquer des cellules iPS sans l’étape d’intégration des 4 gènes par rétrovirus qui modifie le génome des cellules et est vraisemblablement la cause des cancers.
Cependant, la transdifferenciation n’est pas la seule piste plausible : en effet, on pourrait s’interesser a l’enzyme demethylase presente chez les cedres et qui permet le renouvellement cellulaire continu. Mais nous disposons encore que tres peu d’informations sur cette enzyme et les genes qui la codent.



/https%3A%2F%2Fassets.over-blog.com%2Ft%2Fcedistic%2Fcamera.png)
/https%3A%2F%2Fstorage.canalblog.com%2F87%2F62%2F714736%2F50191492_o.jpg)
/https%3A%2F%2Fstorage.canalblog.com%2F34%2F70%2F714736%2F50036832_p.gif)